Tıptaki önemli ilerlemelere karşın kanser, dünya çapında önde gelen ölüm nedenleri arasındadır ve daha uzun yaşam beklentisinin önünde ciddi bir engeldir. Dünya genelinde yılda 20 milyon civarında yeni vaka ve 10 milyon dolayında kansere bağlı ölüm olmaktadır. Örneğin, hayat boyu her sekiz kadından biri (%12), akciğer kanserinden sonra ikinci sıradaki kanser ölüm nedeni olan meme kanserlerine yakalanmaktadır.
Diğer taraftan teknolojideki, bu arada nanoteknolojideki, ilerlemeler baş döndürücü hızla devam ediyor. Tıp alanında bunun en bariz ve güncel örneğini bir insanlık felaketi olarak değerlendirilebilecek SARS-CoV-2 salgınında görmekteyiz. Lipid yapıdaki nanopartiküller, bu virüse karşı tıpta ilk defa rutin kullanıma giren mRNA aşı etken maddesinin hem korunması, hem de hücredeki doğru yere transportu için hayati role sahiptir.
Kanser Oluşum Süreci
Vücudumuzdaki normal hücrelerin kansere dönüşmesi bir takım faktörlere bağlı olarak onkogen, tümör baskılayıcı gen ve DNA tamir geni olarak adlandırılan genlerde art arda meydana gelen mutasyonlar sonucunda olmaktadır.
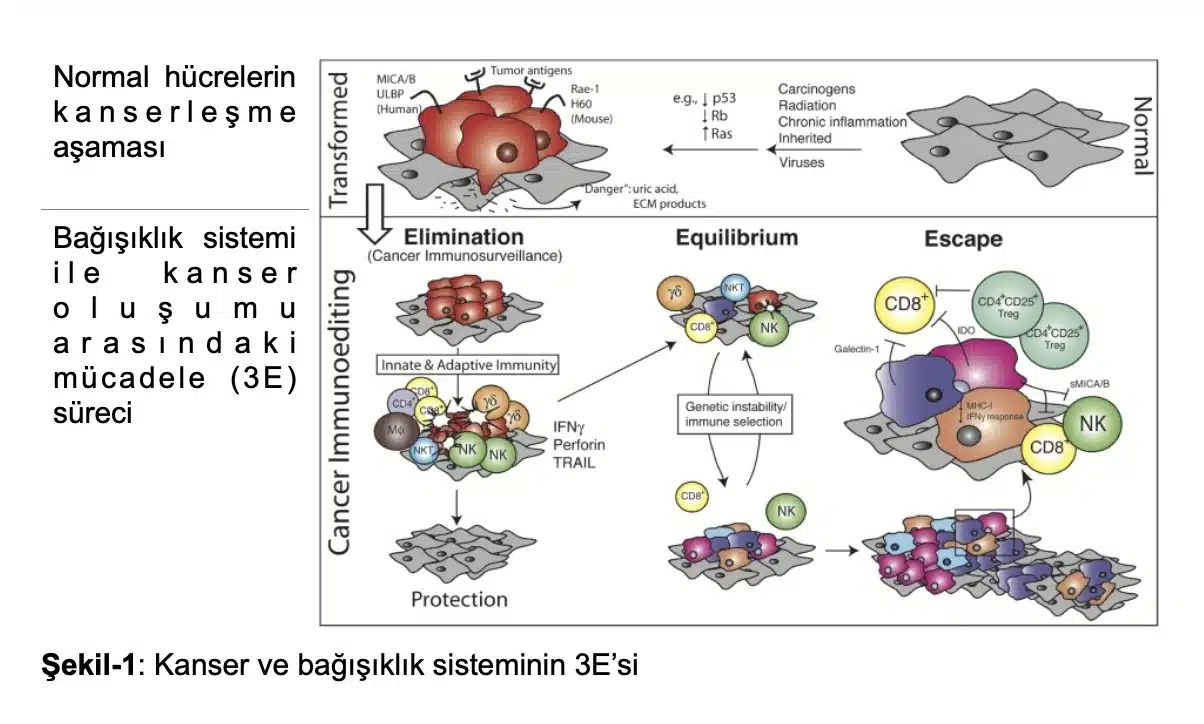
Neyse ki, bağışıklık sistemimiz kanserleşen bu hücrelerle büyük bir mücadele başlatmakta ve büyük çoğunluğunu ilk etapta ortadan kaldırmaktadır. Kanserleşmeye başlayan (transformed) hücrelerle bağışıklık sistemi arasındaki mücadele, İngilizcesi ile 3E olarak belirtebileceğimiz üç aşamada özetlenebilir (Şekil-1):
1. Eliminasyon (bağışıklık sisteminin kanserleşmeye ilk tepkisi),
2. Denge (bağışıklık cevabı ile kanserleşme arasında denge durumu oluşur) ve
3. Kaçış (kanserleşen hücreler bağışık yanıttan kurtulur ve kendisinin hayatta kalıp gelişebileceği uygun bir çevre oluşturur.)
Kanserlerde Tedavi
Kanser tedavisindeki standart yöntemler:
1. Kemoterapi
2. Radyoterapi
3. Cerrahi tedavi
Bu yöntemlerin kanser tedavisindeki yeri çok önemlidir. Ancak diğer taraftan ciddi toksisite, fibrotik doku gelişimi, immün sistemin baskılanmasına bağlı problemler, tedavi direnci gibi çok ciddi yan etkilerinin yapılan yoğun çalışmalara rağmen önüne geçilemediği açıktır.
Kanser tedavilerinde gerçek başarı sağlamanın temel yolu, verilen ilaçların sağlam dokuları etkilemeden mümkün olduğunca kanser hücrelerine ulaşmasına bağlıdır. Bu durum başarıldığında hastanın yaşam kalite ve süresinde büyük ilerleme sağlanacaktır. Bu nedenle aşılar, biyolojik, hormonal, hedeflenmiş ve gen tedavi gibi uygulamalar kanserin türü ve özelliğine göre giderek artan şekilde kullanılmaya başlamıştır.
Tedavide Kullanımı Yönüyle Nanopartiküller
Nanopartikül (NP) olarak adlandırılan maddeler, genel olarak 10-100 nm gibi oldukça küçük boyutta olup, nanoteknolojinin değişik alanlarında kullanılmaktadır. Bu arada üzerine çeşitli maddelerin yüklenebilmeleri özelliği sayesinde kanser tanı ve tedavisi, gen tedavisi, enfeksiyonlar, diş hekimliği gibi tıbbın değişik alanlarında da kullanım alanına sahiptir. Hatta transplantasyon reddini ve transplantasyon sonrası enfeksiyon gelişimini önlemeye yönelik nanopartikül taşıyıcılı uygulamalar da son yıllarda üzerinde durulan çalışmalar arasındadır yer almaktadır
Kendilerine has özellikleri, klasik yöntemlere göre farklı avantajlar kazandırır. Örneğin ikinci kuşak olarak da adlandırılan yönlendirilebilir NP’lerle, üzerine yüklenen bir etken madde istenen bir bölgeye seçici olarak yönlendirilebilmektedir. Dolayısıyla etken madde vücudun diğer bölgelerinden ziyade istenen bölgede daha yoğun konsantrasyonlara ulaşmaktadır. Sonuçta, daha az dozdaki etken madde ile maksimum etki elde edilmekte ve yan etkiler son derece azalmaktadır.
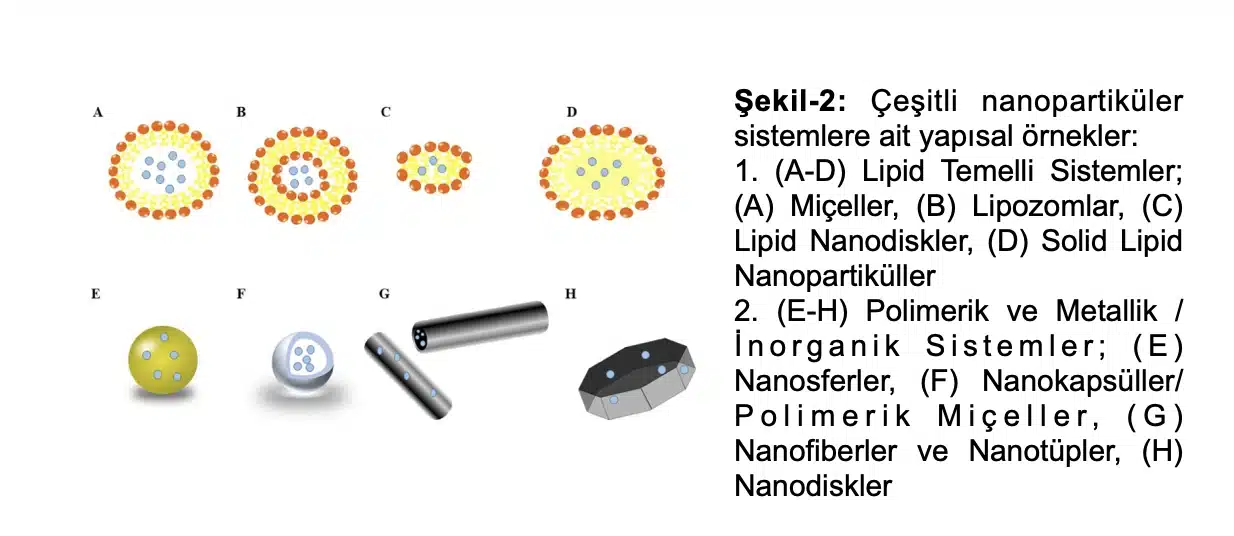
NP’ler; miçel, lipozom, polyester gibi farklı özellikte olabilmektedir. Uygulamada kullanılacak NP’nin boyutu, hazırlanan sistemlerin stabilitesi, üzerine yüklenen maddeyi salım özellikleri, biyodağılımı, etkinliği ve parçalanma ürünlerinin toksik olmaması gibi özellikleri amaca yönelik olarak seçilmektedir (Şekil-2).
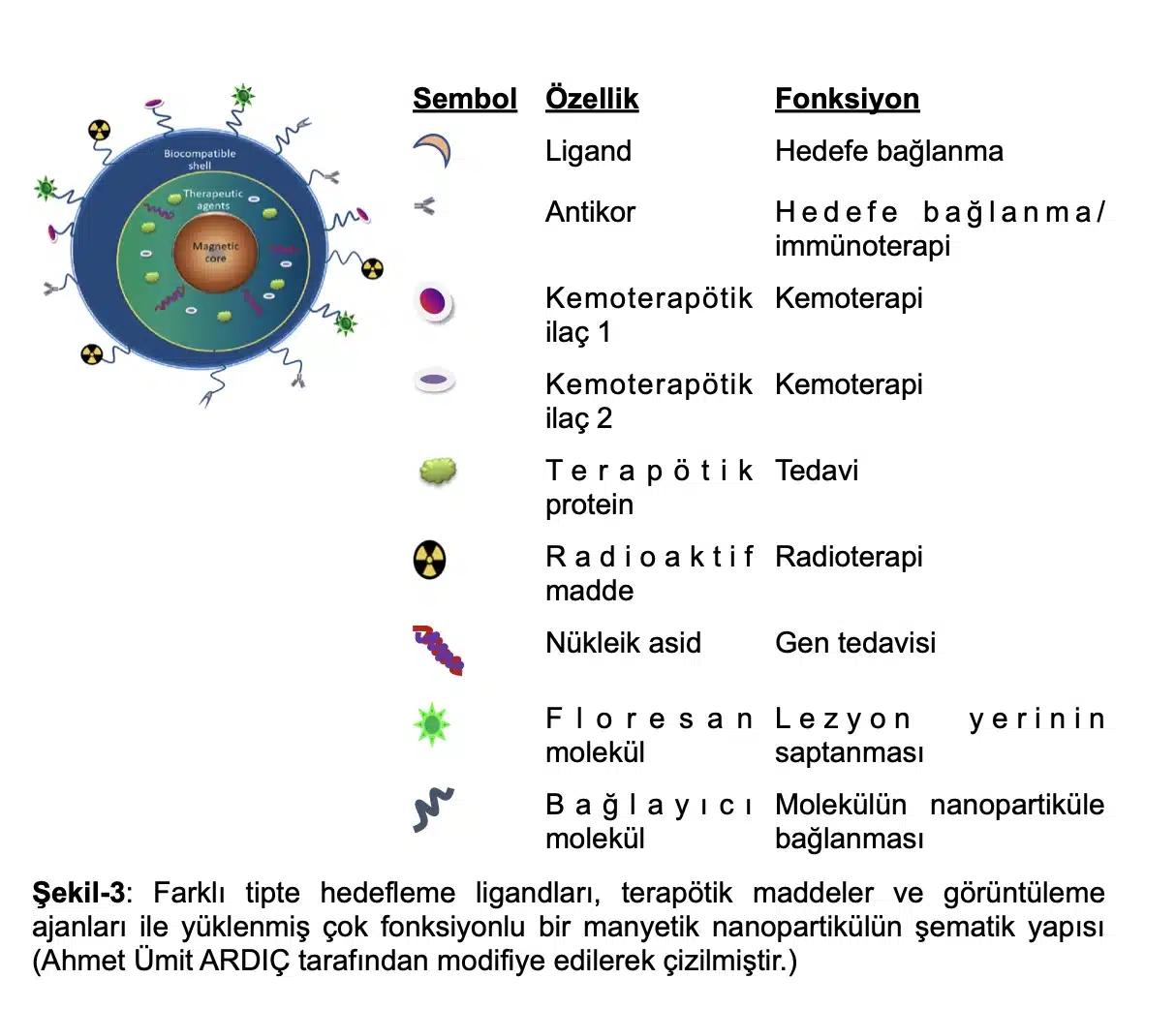
NP’ler amaca uygun olarak toksik ajan, çeşitli ilaçlar, DNA/RNA ve görüntüleme ajanı maddelerle yüklenmektedir. Matriks yapısı, üzerine yüklenecek etken maddenin çözünebilme gibi özelliklerine bağlı olarak bir NP’nin yükleme kapasitesi ve hatta hedef dokuda yüklenen maddeyi salımı değişiklik göstermektedir. Bu kapasitelerine bağlı olarak da çok fonksiyonlu hale getirilebilmektedirler ve bir hastalık oluşumu mekanizması yolağındaki faklı basamaklara yönelik etken maddeler eklenerek tedavide sinerji sağlanabilmektedir. Bunun yanı sıra farklı mekanizma ile etkili olan maddeler eklenerek kombinasyon tedavisi olanağı da doğmaktadır. Yine eklenen biyo-belirteçler sayesinde hedef bölgede akümüle olan ilaç miktarı görüntülenebilmektedir; bu sayede aynı anda tanı ve tedavi olanağı elde edilebilmektedir. Hatta ilaç yüklü NP uygulamalarından sonra bağışıklık sisteminin kanserle mücadelesi daha da hızlanmaktadır (Şekil-3).
Sonuç olarak; nanoonkoloji alanındaki önemli gelişmeler sayesinde, akıllı ilaç uygulama yöntemi olarak da adlandırabileceğimiz hedefleme yoluyla kanser hücrelerine ulaşan ilaç konsantrasyonları arttırılabilmekte ve sağlıklı hücreler üzerine olan toksik etki en aza indirilebilmektedir. Üstelik NP temelli farklı stratejilerle uygulanabilen kombinasyon tedavileri sinerjik etkileri ve yan etkilerin büyük ölçüde azalmasına bağlı olarak önemli bir tedavi potansiyeli taşımaktadır.
Kaynaklar:
Sung H, Ferlay J, Rebecca L, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 0:1–41, 2021.
Mukherjee S, Liang, Veiseh O. Recent Advancements of Magnetic Nanomaterials in Cancer Therapy. Pharmaceutics 12: 147, 2020.
Awasthi R, Roseblade A, Hansbro PM, et al. Nanoparticles in Cancer Treatment: Opportunities and Obstacles. Curr Drug Targets 19:1696-1709, 2018.
Sharma R, Mody N, Agrawal U, et al. Theranostic Nanomedicine; A Next Generation Platform for Cancer Diagnosis and Therapy. Mini Rev Med Chem 17:1746-1757, 2017.
Belyanina I, Kolovskaya O, Zamay S, et al. Targeted Magnetic Nanotheranostics of Cancer. Molecules 22: 975, 2017.
Tiwari G, Tiwari R, Sriwastawa B et al. Drug delivery systems: An updated review. Int J Pharm Investig 2: 2–11, 2012.
Wu M, Huang S. Magnetic nanoparticles in cancer diagnosis, drug delivery and treatment. Molecular And Clinical Oncology 7: 738-746